本土仿制药洗牌加速,大批仿制药面临退市。
日前(8月24日),辽宁省锦州市政府发布《改革完善仿制药供应保障及使用政策的实施意见》
称:对于同品种药品通过仿制药质量和疗效一致性评价的生产企业达到3家以上的
在药品集中采购等方面不再选用未通过仿制药质量和疗效一致性评价的药品。
严格执行辽宁省药品集中采购平台上暂停挂网采购资格的药品和按规定暂不纳入辽宁省药品集中采购范围的药品集中采购政策。
据辽宁省此前(6月11日)发文要求,对于已有3家以上生产企业通过一致性评价的仿制药品种
其他未通过一致性评价的同品种仿制药,即为暂停挂网或暂不纳入集采的对象。

而在辽宁省发文前后,江西、浙江、广西、甘肃也已发文落实“同品种药品通过一致性评价的生产企业达到3家以上的
在药品集中采购等方面不再选用未通过一致性评价的品种”的政策。这意味着,仿制药一致性评价已进入“淘汰赛”环节。
结合距离289目录品种完成一致性评价的“死线“
2018年底,还有4个月,以及“化学药品新注册分类实施前批准上市的其他仿制药自首家品种通过一致性评价后
其他药品生产企业的相同品种原则上应在3年内完成一致性评价;
逾期未完成的,不予再注册”的要求,大批仿制药消亡已成定局。
同步,“三平权”等利好政策也正在全国落地,通过一致性评价的优质仿制药
除了替代原研药外,还将大批替代未通过一致性评价仿制药,抢占其市场空间。
淘汰赛
5省发文,37品种已入局
据健识君梳理,目前全国已有辽宁、江西、浙江、广西、甘肃5省市启动“淘汰”程序。
8月22日,浙江省卫计委就《关于改革完善仿制药供应保障及使用政策的实施意见》征求意见
其中明确:同品种药品,通过一致性评价的生产企业达到3家以上的,
未通过一致性评价的在线交易产品原则上暂停交易资格。
8月10日,广西政府办公厅发布《改革完善仿制药供应保障及使用政策实施方案》明确,
在药品集中采购中,同品种药品通过一致性评价的生产企业未超过3家的,
优先采购通过一致性评价的仿制药,同品种药品通过一致性评价的生产企业达到3家以上的,
不再选用未通过一致性评价的仿制药。
8月6日,甘肃省政府办公厅发布《改革完善仿制药供应保障及使用政策的实施意见》
称,同品种药品通过一致性评价的生产企业达到3家以上的,
在药品集中采购等方面不再选用未通过一致性评价的品种;未超过3家的,
优先采购和使用通过一致性评价的品种。未通过一致性评价的国产同类品种,
其价格原则上不得高于通过一致性评价的药品。
而江西已在集采环节打响了前两枪。
康普药业股份、浙江京新药业股份有限公司、辅仁药业集团有限公司、北京红林制药有限公司的苯磺酸氨氯地平片(5mg);
安徽贝克生物的富马酸替诺福韦二吡呋酯片(300mg)和山东仙河药业蒙脱石散(3g)已在江西暂停挂网。
未来,这一政策有望在全国逐步落地。
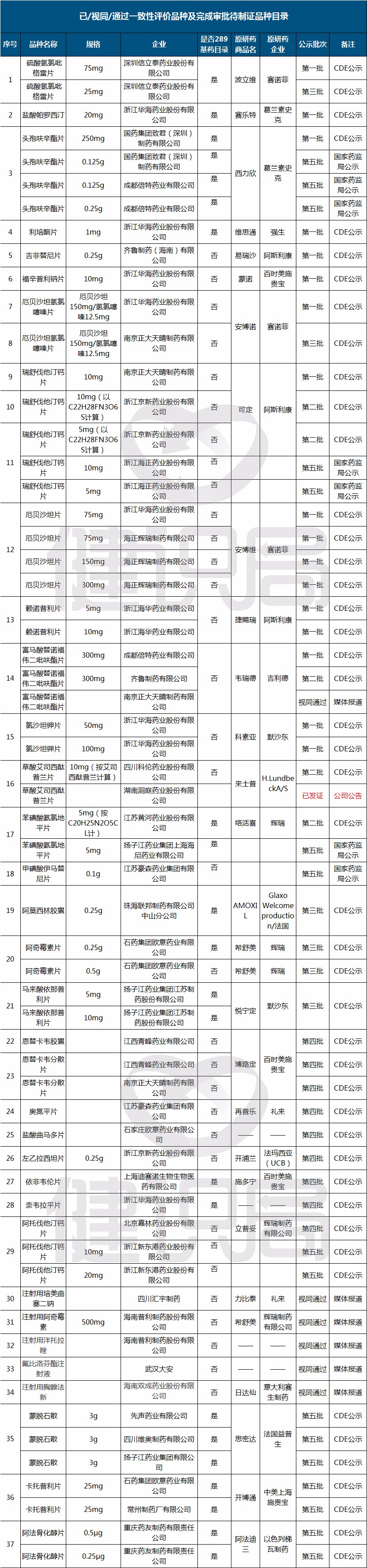
据健识君统计,目前已有37个品种62个药品已通过/视同通过一致性评价。
其中,已有5个品种,有3家生产企业通过了一致性评价。
厄贝沙坦氢氯噻嗪片、厄贝沙坦片、草酸艾司西酞普兰片、恩替卡韦分散片、阿托伐他汀钙片与卡托普利片6个品种则已有两家药企的相应产品通过了一致性评价。也就是说,相关企业将很快进入淘汰赛环节。
“生死线”
8万仿制药批文将消失
已通过/视同通过一致性评价的37个品种中,12个属于“289”品种。
而按照国办2016年8号文(关于开展仿制药质量和疗效一致性评价的意见)要求,
到2018年底,国家基本药物目录(2012年版)中2007年10月1日前批准上市的化学药品仿制药口服固体制剂(289目录品种),应在2018年底前完成一致性评价,其中需开展临床有效性试验和存在特殊情形的品种,
应在2021年底前完成一致性评价;逾期未完成的,不予再注册。
今天,距离这一“死线”,还有大约4个月的时间,也就是说,
4个月内,277个药品要通过一致性评价,以目前进度来看,难度之大,几乎是不可能完成的任务。
而同时,还有一条“死线”――“化学药品新注册分类实施前批准上市的其他仿制药,
自首家品种通过一致性评价后,其他药品生产企业的相同品种原则上应在3年内完成一致性评价;
逾期未完成的,不予再注册”,逼迫已有竞品通过一致性评价的品种,必须加速完成一致性评价,
否则将失去竞争资格,尤其适用于竞争激烈的品种,
如:去年8月份,CFDA摸底结果中,备受企业欢迎的诺氟沙星等14个品种
一致性评价是国产仿制药的“生死劫”。官方数据显示,
约5000家药品制剂生产企业,拥有近17万个药品批文,其中95%是仿制药,行业集中度远低于国际水平。

分析人士指出,由于一致性评价成本较高,单品种耗资在500万到800万不等,
企业会根据自身情况筛选,而后,随着“死线”相继逼近,最终,50%的批文(约8万条)将被淘汰。
根据国办2016年8号文规定,289目录品种应在2018年底完成一致性评价。
而从进度上看,目前通过率不足6%。政策层面,“胡萝卜”和“大棒”并存,
对于部分疗效确切,不良反应/事件发生率低的品种,已有相应豁免政策,
但能否达到促使其尽快“通关”的目的,仍是未知数。
因而,业内人士担忧,恐怕会在一段时间内形成药品短缺。但从长期来看,这样的阵痛在所难免。
| 


